BAVENCIO (avelumab) i kombination med axitinib - Njurcellscancer (RCC)¹
JAVELIN Renal 101, fas 3-studie, randomiserad, öppen multicenterstudie (N=886)
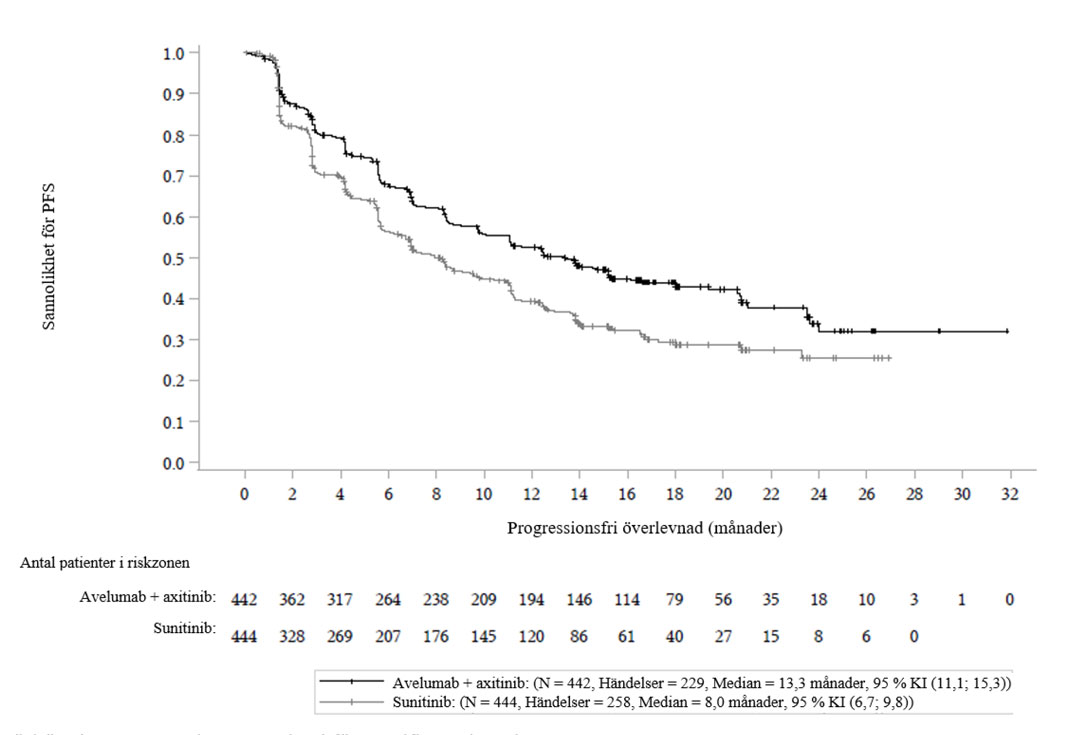
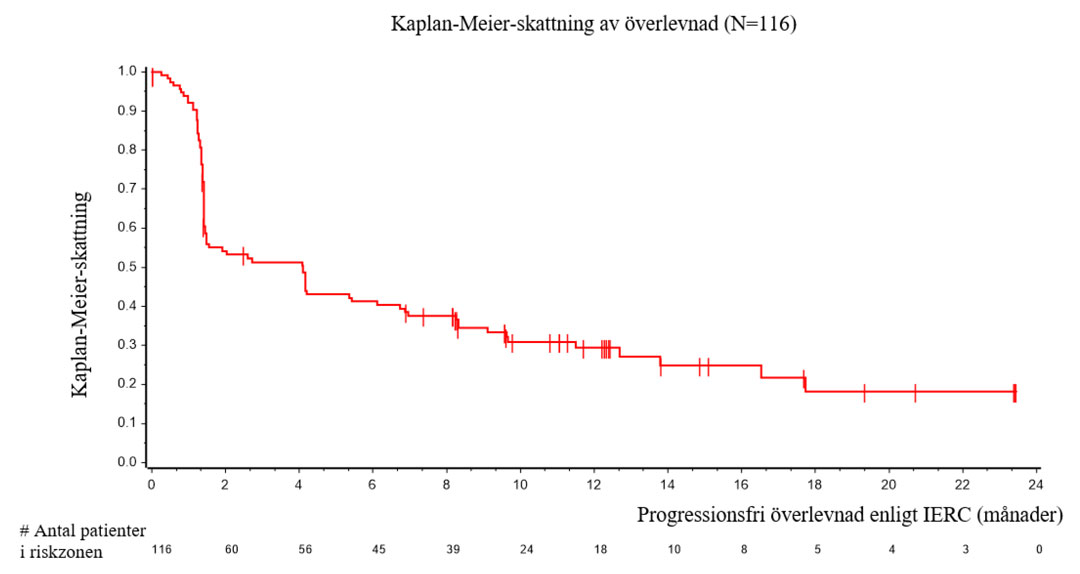
Studien visade statistiskt signifikant progressionsfri överlevnad (progression-free survival, PFS) jämfört med sunitinib som första linjens behandling av vuxna patienter med avancerad njurcancer (RCC) oavsett uttryck av PD-L1 (HR: 0,69 [95% CI: 0,57; 0,83]); Bavencio i kombination med axitinib: 13,3 månader [95% CI: 11,1; 15,3]; sunitinib: 8,0 månader [95% CI: 6,7; 9,8]; p<0,0001). Vidare dubblerades objektiv responsfrekvens (objective response rate, ORR) med Bavencio i kombination med axitinib jämfört med sunitinib i denna population (52,5% [95% CI: 47,7; 57,2] jämfört med 27,3% [95% CI: 23,2; 31,6]).¹
Resultat från JAVELIN Renal 101-studien - ITT-population¹